
Il primo processo e' l'elettrolisi dell'acqua per produrre H2.
Gli attuali elettrolizzatori raggiungono rendimenti del 70-75% come rapporto tra il potere calorifico dell'idrogeno prodotto (11.9 MJ/Nm3) e l'energia elettrica necessaria per produrlo.
Gli attuali elettrolizzatori raggiungono rendimenti del 70-75% come rapporto tra il potere calorifico dell'idrogeno prodotto (11.9 MJ/Nm3) e l'energia elettrica necessaria per produrlo.

Il successivo processo e' la reazione di metanizzazione, che lega l'H2 al CO2 per formare il metano CH4, secondo la reazione di Sabatier :
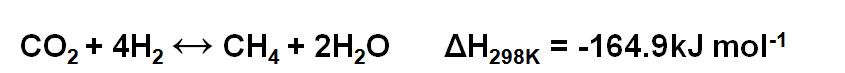
La reazione non necessita di energia aggiuntiva, si autosostiene, e' sicura (2 bar, TRif. 350°C), ha rese elevatissime ed e' economica.
All'uscita del reattore di metanizzazione, i residui di H2 o di CO2 che non hanno reagito possono essere riciclati nel reattore stesso
All'uscita del reattore di metanizzazione, i residui di H2 o di CO2 che non hanno reagito possono essere riciclati nel reattore stesso
Solo per curiosita': l'esperimento e' iniziato da un rattore in tubo di Pyrex con inserito un batuffolo di fibra di
vetro (quella degli acquari) ed una limatura di rame. Per quanto elementare fosse il sistema si e' subito visto
che il gas bruciato all'uscita aveva il classico colore blu del metano!
Quello riportato in figura e' il piccolissimo reattore utilizzato in una seconda fase della sperimentazione
presso l'UNI di Tor Vergata e Roma Tre (Rif. Dr. Igor Luisetto Dipartimento di Scienze UNI Roma Tre) in cui
e' possibile vedere una minima quantita' di catalizzatore commerciale.
Oggi ...
Domani ...


